补充资料:氨
氨
ammonia
氮和氢组成的化合物。化学式NH3。无色有刺鼻臭味的气体,熔点-77.7℃,沸点-33.35℃,密度0.7710克/升。氨很易被液化(临界温度132.9℃,临界压力11.38兆帕)。氨在空气中遇火能爆炸,常温常压下,爆炸极限为16%~28%(体积百分)。
氨分子中HNH的键角是106.75°,分子呈三角锥形。氨分子具有极性,液氨的分子间存在着强的氢键,故液氨中存在缔合分子,并有微弱的电离作用:
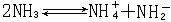 50℃时,电离常数为1.9×10-33。液氨可作有机化合物的溶剂,并能溶解碱金属和钙、锶、钡,如:
50℃时,电离常数为1.9×10-33。液氨可作有机化合物的溶剂,并能溶解碱金属和钙、锶、钡,如:
Na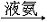 Na++e·xNH3
Na++e·xNH3
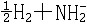
氨极易溶于水,生成的氨水显弱碱性:
 25℃时,电离常数为1×10-5。
25℃时,电离常数为1×10-5。
氨具有还原性,能与氧化剂(如氯)发生反应:
3Cl2+2NH3 N2+6HCl
N2+6HCl
氨分子中的氮原子上有一对孤对电子,能与其他离子或分子形成配位键,与大多数过渡元素离子(如Zn2+、Cd2+、Ag+、Hg2+)结合成配位化合物:
Ag++2NH3 [Ag(NH3) 2]+
[Ag(NH3) 2]+
氨能发生取代反应,生成 一 系列氨的衍生物,如氨基(-NH2)、亚氨基( )的衍生物或氮化物(
)的衍生物或氮化物(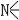 ):
):
HgCl2+2NH3 Hg(NH2)Cl+NH4Cl
Hg(NH2)Cl+NH4Cl
氨的实验室制法是用铵盐与强碱一起加热:
NH4Cl+NaOH NH3+NaCl+H2O
NH3+NaCl+H2O
氨的工业制法是德国F.哈伯1909年发明的,由氮和氢直接合成氨:
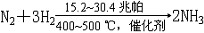 氨也可作为炼焦炉的副产物得到。
氨也可作为炼焦炉的副产物得到。
氨主要用于制造氮肥和复合肥料,有的直接往土壤中施用液氨或氨水,有的将氨转化为硫酸铵、碳酸氢铵、碳酸铵等化肥。氨还是生产硝酸、铵盐、有机中间体、磺胺药、聚氨酯、聚酰胺纤维、丁腈橡胶的原料。由于氨被压缩和冷却到约-33℃时易液化,当它再蒸发为气体时,可从环境吸收大量热,这一性质曾经被用作致冷剂。
ammonia
氮和氢组成的化合物。化学式NH3。无色有刺鼻臭味的气体,熔点-77.7℃,沸点-33.35℃,密度0.7710克/升。氨很易被液化(临界温度132.9℃,临界压力11.38兆帕)。氨在空气中遇火能爆炸,常温常压下,爆炸极限为16%~28%(体积百分)。
氨分子中HNH的键角是106.75°,分子呈三角锥形。氨分子具有极性,液氨的分子间存在着强的氢键,故液氨中存在缔合分子,并有微弱的电离作用:
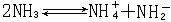 50℃时,电离常数为1.9×10-33。液氨可作有机化合物的溶剂,并能溶解碱金属和钙、锶、钡,如:
50℃时,电离常数为1.9×10-33。液氨可作有机化合物的溶剂,并能溶解碱金属和钙、锶、钡,如:Na
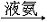 Na++e·xNH3
Na++e·xNH3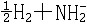
氨极易溶于水,生成的氨水显弱碱性:
 25℃时,电离常数为1×10-5。
25℃时,电离常数为1×10-5。氨具有还原性,能与氧化剂(如氯)发生反应:
3Cl2+2NH3
 N2+6HCl
N2+6HCl氨分子中的氮原子上有一对孤对电子,能与其他离子或分子形成配位键,与大多数过渡元素离子(如Zn2+、Cd2+、Ag+、Hg2+)结合成配位化合物:
Ag++2NH3
 [Ag(NH3) 2]+
[Ag(NH3) 2]+氨能发生取代反应,生成 一 系列氨的衍生物,如氨基(-NH2)、亚氨基(
 )的衍生物或氮化物(
)的衍生物或氮化物(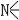 ):
):HgCl2+2NH3
 Hg(NH2)Cl+NH4Cl
Hg(NH2)Cl+NH4Cl氨的实验室制法是用铵盐与强碱一起加热:
NH4Cl+NaOH
 NH3+NaCl+H2O
NH3+NaCl+H2O氨的工业制法是德国F.哈伯1909年发明的,由氮和氢直接合成氨:
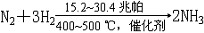 氨也可作为炼焦炉的副产物得到。
氨也可作为炼焦炉的副产物得到。氨主要用于制造氮肥和复合肥料,有的直接往土壤中施用液氨或氨水,有的将氨转化为硫酸铵、碳酸氢铵、碳酸铵等化肥。氨还是生产硝酸、铵盐、有机中间体、磺胺药、聚氨酯、聚酰胺纤维、丁腈橡胶的原料。由于氨被压缩和冷却到约-33℃时易液化,当它再蒸发为气体时,可从环境吸收大量热,这一性质曾经被用作致冷剂。
说明:补充资料仅用于学习参考,请勿用于其它任何用途。
参考词条
 专业词汇(按中图法分类)
专业词汇(按中图法分类)- 马列主义、毛泽东思想、邓小平理论
- 哲学、宗教
- 社会科学总论
- 政治、法律
- 军事
- 经济
- 文化、科学、教育、体育
- 语言、文字
- 文学
- 艺术
- 历史、地理
- 自然科学总论
- 数理科学和化学
- 天文学、地球科学
- 生物科学
- 医药、卫生
- 农业科学
- 工业技术
- 交通运输
- 航空、航天
- 环境科学、安全科学